
Alkoholit ja fenolit (kuten vesi) ovat molemmat heikkoja happoja ja heikkoja emäksiä. Alkoholit voivat toimia Lewisin emäksinä ja protonoitua, jolloin niistä syntyy oksoniumioneja, ROH2+.

Toimiessaan heikkoina happoina alkoholit ja fenolit voivat toimia protonin luovuttajina.

Alkoholit reagoivat alkalimetallien, kuten kaliumin ja natriumin, kanssa muodostaen alkoksideja, jotka ovat vahvoja emäksiä.
|
2 Na
+ 2 CH3OH
|
||
|
|
Natriummetoksidi |
|
|
|
||
|
2
K
+ 2 CH3CH2OH
|
||
|
|
Kaliumetoksidi |
|
Fenolit ovat happamampia kuin alkoholit, koska aromaattinen rengas vetää elektroneja puoleensa ja pystyy jakamaan negatiivisen varauksen aromaattiseen renkaaseen.

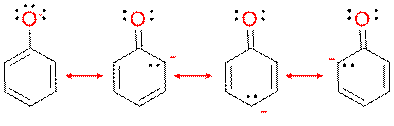
Fenolit liukenevat NaOH:n vesiliuoksiin, jolloin syntyy fenoksidi-ioneja.

Substituoidut fenolit voivat olla happamampia tai emäksisempiä kuin fenoli. Fenolissa oleva elektroneja puoleensa vetävä substituentti, esim. nitro-ryhmä, lisää fenolin happamuutta. Vastaavasti fenoli, joka sisältää elektroneja luovuttavan ryhmän, esim. alkyyliryhmän, on vähemmän hapan.
|
Elektroneja luovuttavia substituentteja |
Elektroneja puoleensa vetäviä substituentteja |
|
|
 |
Nimi
kaava
pKa
t-butyylialkoholi
(CH3)3COH
18
etanoli
CH3CH2OH
16
metanoli
CH3OH
15.5
vesi
H2O
15.74
2,2,2-trifluorietanoli
CF3CH2OH
12.4
p-metyylifenoli
CH3C6H4OH
10.17
fenoli
C6H5OH
9.89
p-nitrofenoli
NO2C6H4OH
7.15
Tehtävä 1. Kumpi on happamampi, p-metyylifenoli vai p-syanofenoli?
Tehtävä 2. Aseta seuraavat yhdisteet kasvavan happamuuden mukaiseen järjestykseen:
bentsyylialkoholi, p-bromifenoli, 2,4-dibromifenoli, p-metoksifenoli.
| Sisällysluettelo | 8. Alkoholit, eetterit ja fenolit |