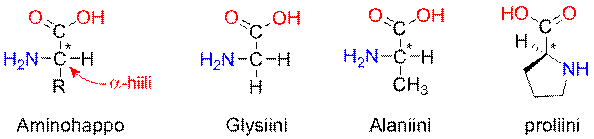
Aminohapot sisältävät sekä emäksisen aminoryhmän että happaman karboksyyliryhmän.

Aminohapot ne muodostavat molekyylin sisäisiä suoloja eli ne esiintyvät kahtaisioneina protonin siirtyessä karboksyyliryhmästä aminoryhmään.
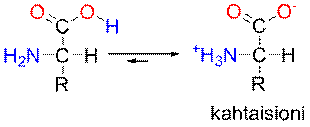
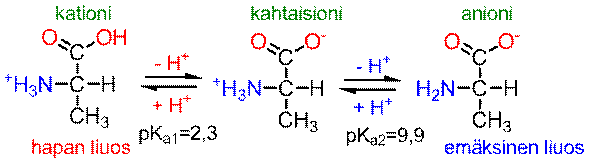
Aminohapot ovat amfolyyttejä eli ne pystyvät toimimaan sekä happoina että emäksinä. Happamassa liuoksessa aminohappo toimii emäksenä, jolloin COO– -ryhmä ottaa vastaan protonin:
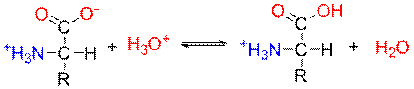
Vastaavasti emäksisessä liuoksessa aminohapon ammonium-ryhmä luovuttaa protonin hydroksidi-ionille:
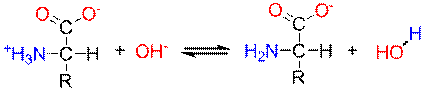
Aminohappojen karboksyyliryhmän pKa vaihtelee aminohaposta riippuen välillä 2,1± 0,5 (happamampi kuin etikkahapon, jonka pKa on 4,8). Protonoituneen aminoryhmän (NH3+) pKa on yli 9.
Happamassa liuoksessa aminohappo on protonoitunut ja esiintyy kationina; emäksisessä liuoksessa vastaavasti anionina. Näiden muotojen välillä on olemassa pH-arvo, jossa aminohappo esiintyy kahtaisionisena molekyylinä. Tätä pH-arvoa sanotaan isoelektriseksi pisteeksi. Aminohapoilla, joissa on neutraali sivuketju, isoelektrinen piste on pH-välillä 5,0-6,5. Esimerkiksi alaniini isoelektrinen piste on 6.00, jossa pH:ssa se on täydellisesti kahtaisionimuodossa.
Tässä pH:ssa liuos on ulospäin sähköisesti neutraali. Käytännössä aminohapot esiintyvät kahtaisionimuodossa pKa-arvojen pH-välillä eli esim. alaniinin aminoryhmä on ionimuodossa kun pH < 9,9 (=pKa2) ja vastaavasti karboksyyliryhmä on anionimuodossa kun pH > 2,3 (=pKa1).
Alla olevassa kuvaajassa on esitetty protonoituneen aminohapon titraus emäksellä. Kun yksi ekvivalentti emästä (OH- ) on lisätty, on karboksyyliryhmä täydellisesti deprotonoitunut. Tämä on titrauksen ekvivalenttikohta ja samalla glysiinin isoelektrinen piste (pI), joka voidaan myös laskea pKa -arvojen keskiarvona: pI = (pKa1+ pKa2)/2 = (2,3 + 9,6)/2 = 5,95.
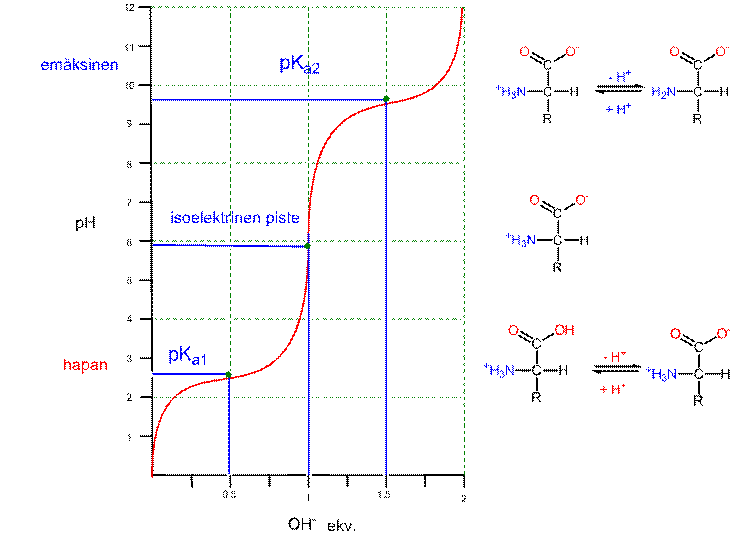
Tehtävä. Glysiinin pKa arvot ovat: pKa1 = 2,3 ja pKa2 = 9,6. Piirrä glysiinin rakenteet pH:ssa 2,0, pH:ssa 6,0 ja pH:ssa 10,0.
| Sisällysluettelo |